Cảnh báo về một số loại thuốc giả, nghi giả, không rõ nguồn
| Cảnh báo thuốc giả Salonpas Gel Bộ Y tế đề nghị tăng cường thanh tra, kiểm tra, phòng chống thuốc giả Cảnh báo phát hiện 4 lô thuốc Ophazidon giả Cảnh báo về việc thuốc giả Phong tê nhức Hổ Cốt Hoàn |
Theo đó, Cục Quản lý Dược nhận được một số thông tin của Cơ quan Cảnh sát điều tra, Công An huyện Thạch Thất, Công ty TNHH AstraZeneca Việt Nam, Công ty TNHH Novartis Việt Nam, Văn phòng đại diện F.Hoffmann-La Roche Ltd tại Hà Nội, Văn phòng đại diện Les Kaboratoires Servier tại Hà Nội về việc phát hiện một số lô thuốc giả, nghi ngờ giả, không rõ nguồn gốc.
Số thuốc này có thông tin ghi trên nhãn (hình ảnh đính kèm) như sau: Nexium 40mg, Enterik Kapli Pellet Tablet, AstraZeneca, (01) 08699786040045, (21) 3500000157639358; (17) SKT: 09.2024; (10) Parti no: 22B264. Trong mỗi hộp có 4 vỉ, mỗi vỉ 7 viên.
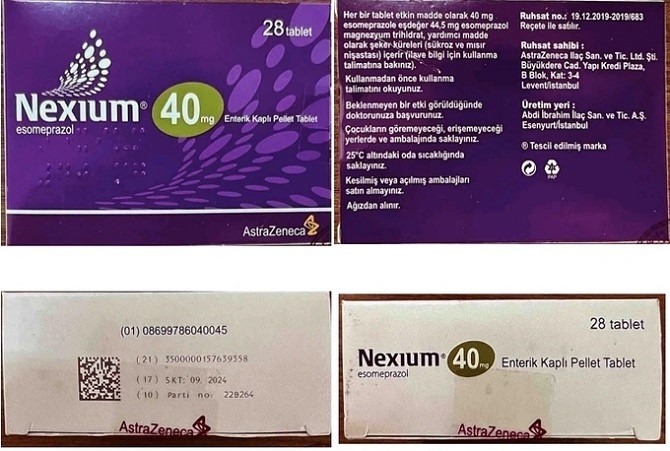 |
| Mẫu thuốc Nexium (Ảnh: Cục Quản lý Dược) |
Nexium 40mg, Enterik Kapli Pellet Tablet, AstraZeneca, Số lô: 21H979, trong mỗi hộp có 4 vỉ, mỗi vỉ 7 viên (hình ảnh giống với hình ảnh của lô Parti no: 22B264 nêu trên).
Tetracyclin Tw3 250mg, SĐK: VD-28109-17, Số lô SX: 0321, NSX: 2/2/2021, HD: 2/2/2024, Nhà sản xuất: Công ty Cổ phần dược phẩm Trung ương 3, quy cách hộp 400 viên nén.
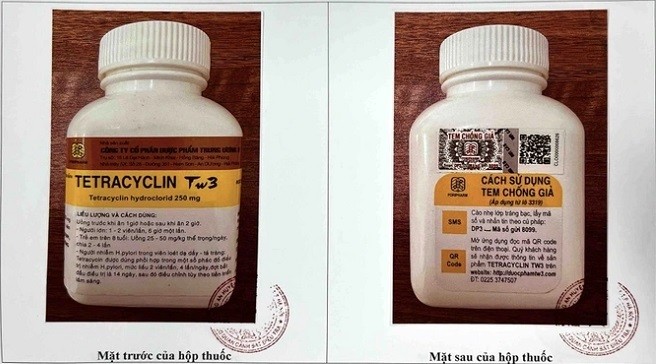 |
| Mẫu thuốc Tetracyclin Tw3 (Ảnh: Cục Quản lý Dược) |
Clorocid Tw3 250mg, SĐK: VD-25305-16, Số lô SX: 0321, NSX: 7/7/2021, HD: 7/7/2024, Nhà sản xuất: Công ty Cổ phần dược phẩm Trung ương 3, qui cách hộp 400 viên nén.
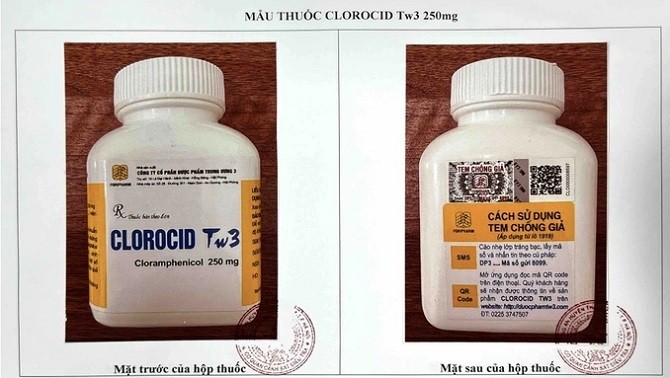 |
| Mẫu thuốc Clorocid Tw3 (Ảnh: Cục Quản lý Dược) |
Công ty CP Dược phẩm Trung ương 3 thông báo tới Cục Quản lý Dược từ ngày 16/9/2019 đến 29/6/2022 (thời điểm công ty thông báo), công ty không tiến hành sản xuất lô thuốc nào đối với Clorocid Tw3, SĐK: VD-25305-16.
Tiếp đến là các loại thuốc: TobraDex, hộp 1 lọ đếm giọt Droptainer 5ml, số lô: 22C10HB, ngày hết hạn/EXP: 10/3/2024, ngày sản xuất/ MFD: 10/3/2022; Tecentriq 1200mg/20ml (atezolizumab), số lô B0033B03, HSD: 2/9/24, code 10001437939658; Diamicron MR 30mg, số lô: 695986, HSD: 9/2024; Coveram 5mg/5mg, số lô: 2170310010, HSD: 11/2024.
Để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc không kinh doanh, phân phối và sử dụng các sản phẩm được liệt kê có các đặc điểm để phân biệt nêu trên, báo cáo cơ quan chức năng nếu phát hiện lô thuốc trên.
Các đơn vị cần tăng cường việc thanh tra, kiểm tra hoạt động kinh doanh của các cơ sở kinh doanh dược trên địa bàn, tập trung việc kiểm tra đối với các sản phẩm có thông tin như mô tả nêu trên.
Đồng thời, các đơn vị tiếp nhận và xác minh thông tin, báo cáo Ban chỉ đạo 389 tỉnh, thành phố và phối hợp với các cơ quan chức năng liên quan kiểm tra xác minh, truy tìm nguồn gốc xuất xứ đối với các sản phẩm có thông tin như mô tả nêu trên nếu phát hiện trên địa bàn.
Ngoài ra, các đơn vị cũng cần khẩn trương tiến hành thanh tra, kiểm tra hoạt động kinh doanh thuốc đối với các cơ sở kinh doanh, sử dụng thuốc nêu trên; xử lý nghiêm các trường hợp vi phạm và báo cáo kết quả về Cục Quản lý Dược.
Cục cũng yêu cầu các công ty sản xuất, kinh doanh, nhập khẩu, phân phối liên quan đến các sản phẩm có thông tin như mô tả nêu trên cung cấp thông tin và phối hợp với Sở Y tế các tỉnh, thành phố và các cơ quan chức năng có liên quan trong việc truy tìm nguồn gốc đối với các sản phẩm có thông tin như mô tả nêu trên.
Tin liên quan
Cùng chuyên mục
Đọc thêm
 Tin Y tế
Tin Y tế
Ngành Y tế bảo đảm công tác cấp cứu, phòng dịch thông suốt
 Tin Y tế
Tin Y tế
Những phòng cấp cứu “sáng đèn” xuyên Tết
 Tin Y tế
Tin Y tế
Phát huy vai trò các bệnh viện tuyến cuối "giành giật sự sống, là hy vọng lớn nhất của người bệnh"
 Tin Y tế
Tin Y tế
Bồn sinh dưới nước ấm trong thai sản trọn gói Luxury PhenikaaMec: Khi khoa học hiện đại nâng niu trải nghiệm sinh nở của người mẹ
 Xã hội
Xã hội
Sun Group tài trợ gói thiết bị y tế trị giá 12 tỷ đồng cho Trung tâm y tế Tương Dương
 Tin Y tế
Tin Y tế
Vinmec phẫu thuật tạo hình hộp sọ thành công cho bệnh nhi 10 tháng tuổi mắc dị tật hiếm gặp
 Tin Y tế
Tin Y tế
Phối hợp bảo đảm an ninh, trật tự trong lĩnh vực y tế
 Tin Y tế
Tin Y tế
234 cơ sơ bán lẻ đăng ký trực bán thuốc dịp Tết Nguyên đán
 Tin Y tế
Tin Y tế
Tăng cường kiến thức chuyên môn về vi rút Nipah cho nhân viên y tế
 Tin Y tế
Tin Y tế















